Gitelman综合征合并焦磷酸钙沉积病一例
+关注
Gitelman综合征(Gitelman syndrome,GS)是一种罕见的常染色体隐性遗传疾病,以低钾血症、代谢性碱中毒,伴低镁血症和低钙尿为特征的肾小管疾病。病因是编码位于肾脏远曲小管上皮顶端膜的噻嗪类敏感钠氯协同转运蛋白(sodium chloride co-transporter,NCC)的SLC12A3基因失活突变[1]。GS患者的常见症状包括夜尿增多,广泛的肌肉症状,如肌肉无力、痛性痉挛,少见手足搐搦和横纹肌溶解症,多达50%的患者出现关节疼痛,少数患者会表现为生长迟缓、软骨钙化[1-2]。本文报道1例GS合并焦磷酸钙沉积病(calcium pyrophosphate deposition,CPPD)病例,以提高临床医生对该罕见病骨关节表现的认识。
1、病例摘要
患者,男性,58岁,因“多关节肿痛15年余,间断四肢无力7年,加重7月”于2020年9月至北京协和医院风湿免疫科就诊。患者自2005年起无明显诱因出现双膝关节肿痛,予以对症处理后好转,之后间断发作上述症状。2013年患者突发四肢软瘫,自诉于外院查血钾降低,予补钾治疗后四肢无力症状缓解。后就诊于本院内分泌科,查血钾(K)2.4 mmol/L(3.5~5.5 mmol/L),镁(Mg)0.55 mmol/L(0.70~1.10 mmol/L),钙(Ca)2.21 mmol/L(2.13~2.70 mmol/L),24小时尿钾77.1 mmol,血管紧张素Ⅱ(立位):130.39 pg/mL(25.3~145.3 pg/ml),肾素活性(立位):1.72 ng·mmol-1·L-1(0.93~6.56 ng·mmol-1·L-1);血醛固酮(立位):11.76 ng/dl(6.5~29.6 ng/dL);肾上腺CT未见明显异常。予以口服补钾治疗。患者之后未规律诊治,仍间断出现四肢无力,补钾后缓解,期间患者仍间断发作膝关节肿痛。2019年11月于本院骨科查膝关节X线:双膝关节软骨钙质沉积,轻度骨质增生,关节外侧间隙变窄(图1A);踝关节X线:双侧外踝关节软骨钙化(图1B)。继续予非甾体类抗炎药对症治疗。2020年2月患者无明显诱因出现双腕关节、双手近端指间关节、双肘关节、双肩关节肿痛,予非甾体抗炎药治疗后症状可缓解,后仍反复发作。2020年9月1日起就诊于本院,查体:双手近端关节、双腕关节明显压痛,左肩关节抬举受限,双膝关节肿胀伴压痛。进一步查血K 2.9 mmol/L,血Mg 0.50 mmol/L,血尿酸(UA)243 μmol/L;动脉血气(自然状态):pH 7.46(7.35~7.45),pO2 85 mmHg(83-108 mmHg),pCO2 41 mmHg(35~45 mm Hg),HCO3- 28.7 mmol/L(22.0~27.0 mmol/L),BE 4.9 mmol/L(-3.0~+3.0 mmol/L);血沉(ESR)13 mm/h,超敏C反应蛋白(hsCRP)2.19 mg/L;类风湿因子(RF)、抗环胍氨酸多肽(CCP)抗体、抗核抗体谱17项均(-)。腕关节X线:双侧桡腕关节、桡尺关节处少许云雾状影存在,舟月骨之间可见条状高密度沉积物(图1C);左肩关节X线:左侧肱骨头骨质增生,软骨处条状环形钙化,关节囊钙化(图1D);膝关节超声:膝关节关节软骨略变薄伴条状钙化(图2)。结合患者关节症状及影像学检查结果,考虑诊断CPPD,进一步行基因检测提示患者存在SLC12A3基因c.791C>G和c.1084A>G复合杂合突变,提示Gitelman综合征诊断明确。治疗方面,予得宝松1支肌注,依托考昔 60 mg,每日1次口服;加用氯化钾缓释片1.5 g,每天3次口服;门冬氨酸钾镁(潘南金)4片,每天3次口服;枸橼酸钾口服溶液20 ml,每天3次口服。监测患者血K能上升至3.7 mmol/L,血Mg上升至0.76 mmol/L,患者关节肿痛症状明显缓解。之后患者在本科门诊长期随诊至今,一直积极口服补充钾镁,逐渐减停依托考昔,未再发作关节肿痛。

图1 患者受累关节的X线表现
A.双膝关节X线:双膝关节软骨钙质沉积,轻度骨质增生,关节外侧间隙变窄;B.踝关节X线:双侧外踝关节软骨钙化;C.双腕关节X线:双侧桡腕关节、桡尺关节处少许云雾状影存在,舟月骨之间可见条状高密度沉积物;D.左肩关节X线:左侧肱骨头骨质增生,软骨处条状环形钙化,关节囊钙化(异常所见以白色箭头标注)
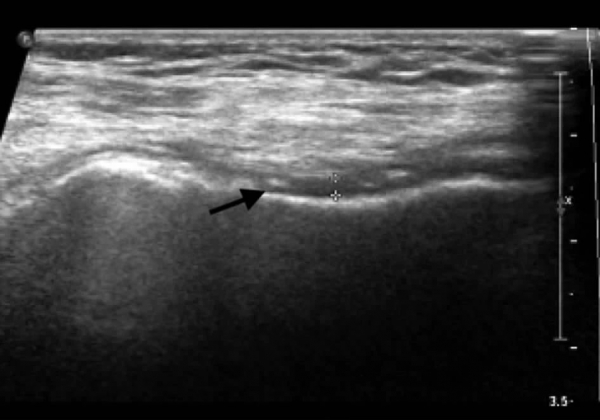
图2 膝关节超声示关节软骨略变薄伴条状钙化(黑色箭头)
2、讨论
本文报告1例罕见的GS合并CPPD的患者。该患者关节病变迁延10年余,结合其典型的影像学表现,考虑CPPD诊断明确。CPPD主要是由于焦磷酸钙晶体沉积于关节所致,CPPD主要见于60岁以上的老年人群,可表现为急性关节炎发作(假性痛风),也可以表现为慢性关节病变[3-4]。本例患者在中青年时即发作关节症状,考虑并非CPPD的好发年龄范围,因此需进一步分析有无可能导致CPPD的继发因素。结合该患者有明确的低钾血症和低镁血症,血气分析提示存在代谢性碱中毒,基因检测提示存在SLC12A3基因复合杂合突变,提示Gitelman综合征诊断明确。
对于CPPD患者,需注意筛查潜在的遗传或代谢方面的危险因素,如低磷酸酶血症、甲状旁腺功能亢进症、血色素沉着症和低镁血症,对于家族聚集性的病例还需筛查基因[3-4]。GS作为一种罕见病,主要临床表现为慢性低钾血症、低镁血症、代谢性碱中毒和低尿钙症,该病早期诊断常存在困难,特别应该和Bartter综合征进行鉴别。GS的确诊主要是基于典型的临床表现和和基因检测(金标准,即SLC12A3基因突变)[1]。关于GS患者合并CPPD,既往国外文献中已有一些相关的个案报道,但考虑到CPPD可表现为无症状,因此GS患者中实际合并CPPD的情况可能会被临床医生低估[5-11]。低镁血症是GS常见的临床表现,镁离子是组织非特异性碱性磷酸酶的重要激活剂,该磷酸酶能将焦磷酸水解为无机磷酸盐,从而增加焦磷酸钙晶体的溶解度。因此低镁血症可能促进关节中焦磷酸钙晶体的形成,从而导致CPPD[5-7,11-12]。此外,肾钙重吸收增加也可能有助于钙沉积[13]。综上,对于该患者的诊断,从一元论角度考虑,GS为导致CPPD的原因。
关于CPPD的治疗,急性关节炎时主要以控制炎症为主,而对于该病的长期控制,若有明确的诱因,则首先纠正相关的诱因[14]。针对本患者,考虑GS所致的低镁血症为导致CPPD的诱因。根据2021年版GS诊疗中国专家共识,合并低镁血症时,可考虑积极口服补镁治疗,通常认为GS患者合适的血镁水平为0.6 mmol/L[15]。该患者入院后存在关节肿痛,予肌注得保松和口服依托考昔后关节症状好转,之后经积极口服门冬氨酸钾镁后,随访2年以上时间,未再发作关节肿痛症状,因此考虑补镁治疗可有效控制患者的CPPD。考虑到该患者GS为基因突变所致,因此该患者需终身电解质替代治疗。
综上,风湿免疫科医生在诊治CPPD患者时,应注意筛查可能的诱因,避免漏诊误诊,并在治疗时需对诱因行积极纠正。
参考文献:略
作者:金可涵,张磊,周慷,吴婵媛,周佳鑫,李梦涛,赵岩,曾小峰
来源:中华临床免疫和变态反应杂志 公众号
( 转载文章系出于传递学术分享之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请通过 邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。)
2024-04-17 14:45:07 8351 浏览
1、病例摘要
患者,男性,58岁,因“多关节肿痛15年余,间断四肢无力7年,加重7月”于2020年9月至北京协和医院风湿免疫科就诊。患者自2005年起无明显诱因出现双膝关节肿痛,予以对症处理后好转,之后间断发作上述症状。2013年患者突发四肢软瘫,自诉于外院查血钾降低,予补钾治疗后四肢无力症状缓解。后就诊于本院内分泌科,查血钾(K)2.4 mmol/L(3.5~5.5 mmol/L),镁(Mg)0.55 mmol/L(0.70~1.10 mmol/L),钙(Ca)2.21 mmol/L(2.13~2.70 mmol/L),24小时尿钾77.1 mmol,血管紧张素Ⅱ(立位):130.39 pg/mL(25.3~145.3 pg/ml),肾素活性(立位):1.72 ng·mmol-1·L-1(0.93~6.56 ng·mmol-1·L-1);血醛固酮(立位):11.76 ng/dl(6.5~29.6 ng/dL);肾上腺CT未见明显异常。予以口服补钾治疗。患者之后未规律诊治,仍间断出现四肢无力,补钾后缓解,期间患者仍间断发作膝关节肿痛。2019年11月于本院骨科查膝关节X线:双膝关节软骨钙质沉积,轻度骨质增生,关节外侧间隙变窄(图1A);踝关节X线:双侧外踝关节软骨钙化(图1B)。继续予非甾体类抗炎药对症治疗。2020年2月患者无明显诱因出现双腕关节、双手近端指间关节、双肘关节、双肩关节肿痛,予非甾体抗炎药治疗后症状可缓解,后仍反复发作。2020年9月1日起就诊于本院,查体:双手近端关节、双腕关节明显压痛,左肩关节抬举受限,双膝关节肿胀伴压痛。进一步查血K 2.9 mmol/L,血Mg 0.50 mmol/L,血尿酸(UA)243 μmol/L;动脉血气(自然状态):pH 7.46(7.35~7.45),pO2 85 mmHg(83-108 mmHg),pCO2 41 mmHg(35~45 mm Hg),HCO3- 28.7 mmol/L(22.0~27.0 mmol/L),BE 4.9 mmol/L(-3.0~+3.0 mmol/L);血沉(ESR)13 mm/h,超敏C反应蛋白(hsCRP)2.19 mg/L;类风湿因子(RF)、抗环胍氨酸多肽(CCP)抗体、抗核抗体谱17项均(-)。腕关节X线:双侧桡腕关节、桡尺关节处少许云雾状影存在,舟月骨之间可见条状高密度沉积物(图1C);左肩关节X线:左侧肱骨头骨质增生,软骨处条状环形钙化,关节囊钙化(图1D);膝关节超声:膝关节关节软骨略变薄伴条状钙化(图2)。结合患者关节症状及影像学检查结果,考虑诊断CPPD,进一步行基因检测提示患者存在SLC12A3基因c.791C>G和c.1084A>G复合杂合突变,提示Gitelman综合征诊断明确。治疗方面,予得宝松1支肌注,依托考昔 60 mg,每日1次口服;加用氯化钾缓释片1.5 g,每天3次口服;门冬氨酸钾镁(潘南金)4片,每天3次口服;枸橼酸钾口服溶液20 ml,每天3次口服。监测患者血K能上升至3.7 mmol/L,血Mg上升至0.76 mmol/L,患者关节肿痛症状明显缓解。之后患者在本科门诊长期随诊至今,一直积极口服补充钾镁,逐渐减停依托考昔,未再发作关节肿痛。

图1 患者受累关节的X线表现
A.双膝关节X线:双膝关节软骨钙质沉积,轻度骨质增生,关节外侧间隙变窄;B.踝关节X线:双侧外踝关节软骨钙化;C.双腕关节X线:双侧桡腕关节、桡尺关节处少许云雾状影存在,舟月骨之间可见条状高密度沉积物;D.左肩关节X线:左侧肱骨头骨质增生,软骨处条状环形钙化,关节囊钙化(异常所见以白色箭头标注)

图2 膝关节超声示关节软骨略变薄伴条状钙化(黑色箭头)
2、讨论
本文报告1例罕见的GS合并CPPD的患者。该患者关节病变迁延10年余,结合其典型的影像学表现,考虑CPPD诊断明确。CPPD主要是由于焦磷酸钙晶体沉积于关节所致,CPPD主要见于60岁以上的老年人群,可表现为急性关节炎发作(假性痛风),也可以表现为慢性关节病变[3-4]。本例患者在中青年时即发作关节症状,考虑并非CPPD的好发年龄范围,因此需进一步分析有无可能导致CPPD的继发因素。结合该患者有明确的低钾血症和低镁血症,血气分析提示存在代谢性碱中毒,基因检测提示存在SLC12A3基因复合杂合突变,提示Gitelman综合征诊断明确。
对于CPPD患者,需注意筛查潜在的遗传或代谢方面的危险因素,如低磷酸酶血症、甲状旁腺功能亢进症、血色素沉着症和低镁血症,对于家族聚集性的病例还需筛查基因[3-4]。GS作为一种罕见病,主要临床表现为慢性低钾血症、低镁血症、代谢性碱中毒和低尿钙症,该病早期诊断常存在困难,特别应该和Bartter综合征进行鉴别。GS的确诊主要是基于典型的临床表现和和基因检测(金标准,即SLC12A3基因突变)[1]。关于GS患者合并CPPD,既往国外文献中已有一些相关的个案报道,但考虑到CPPD可表现为无症状,因此GS患者中实际合并CPPD的情况可能会被临床医生低估[5-11]。低镁血症是GS常见的临床表现,镁离子是组织非特异性碱性磷酸酶的重要激活剂,该磷酸酶能将焦磷酸水解为无机磷酸盐,从而增加焦磷酸钙晶体的溶解度。因此低镁血症可能促进关节中焦磷酸钙晶体的形成,从而导致CPPD[5-7,11-12]。此外,肾钙重吸收增加也可能有助于钙沉积[13]。综上,对于该患者的诊断,从一元论角度考虑,GS为导致CPPD的原因。
关于CPPD的治疗,急性关节炎时主要以控制炎症为主,而对于该病的长期控制,若有明确的诱因,则首先纠正相关的诱因[14]。针对本患者,考虑GS所致的低镁血症为导致CPPD的诱因。根据2021年版GS诊疗中国专家共识,合并低镁血症时,可考虑积极口服补镁治疗,通常认为GS患者合适的血镁水平为0.6 mmol/L[15]。该患者入院后存在关节肿痛,予肌注得保松和口服依托考昔后关节症状好转,之后经积极口服门冬氨酸钾镁后,随访2年以上时间,未再发作关节肿痛症状,因此考虑补镁治疗可有效控制患者的CPPD。考虑到该患者GS为基因突变所致,因此该患者需终身电解质替代治疗。
综上,风湿免疫科医生在诊治CPPD患者时,应注意筛查可能的诱因,避免漏诊误诊,并在治疗时需对诱因行积极纠正。
参考文献:略
作者:金可涵,张磊,周慷,吴婵媛,周佳鑫,李梦涛,赵岩,曾小峰
来源:中华临床免疫和变态反应杂志 公众号
( 转载文章系出于传递学术分享之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请通过 邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。)

 抢沙发,发首评,稳占C位!
立即抢沙发
抢沙发,发首评,稳占C位!
立即抢沙发




