中药审评审批改革重磅事件!国家药监局成立委员会,这些院士都在委员名单!
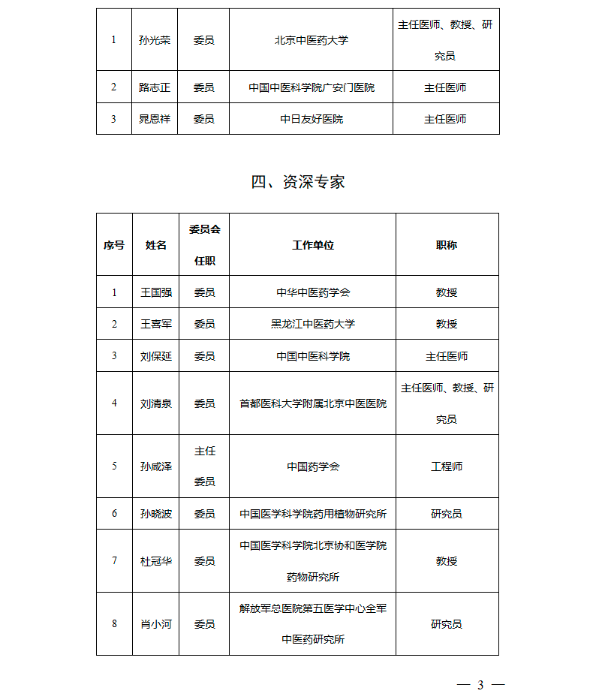
专委会主任委员为孙咸泽,副主任委员为张伯礼、黄璐琦、王辰,秘书处设在国家药监局药品注册管理司。主任委员、副主任委员、委员任期3年。(专委会名单见文末)
国家药监局此前未曾成立过以“战略决策”为特征的专家咨询委员会。专委会规格之高,也超出以往,体现了对中药监管工作的高度重视。
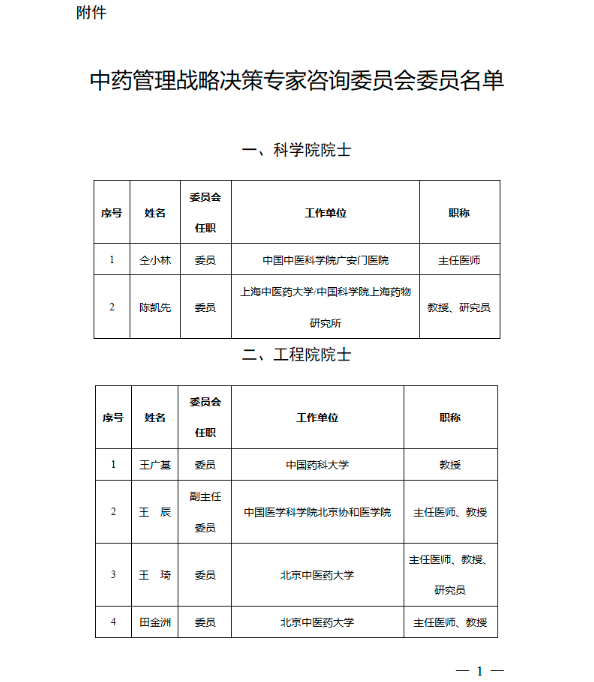
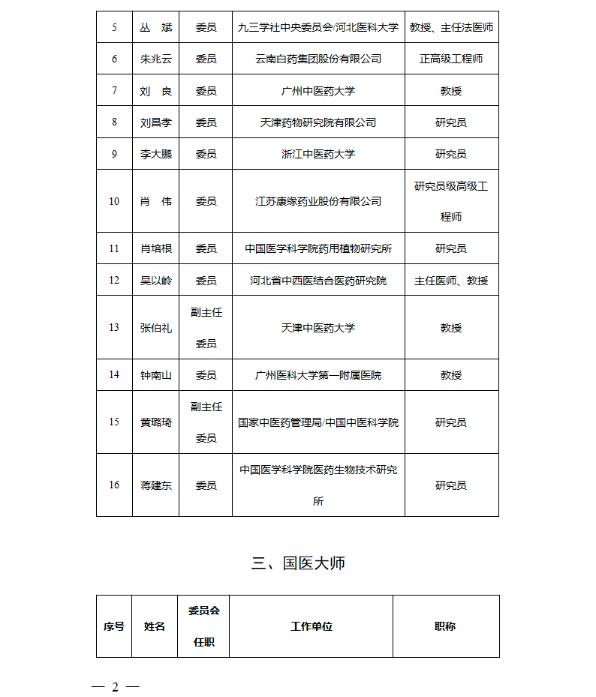
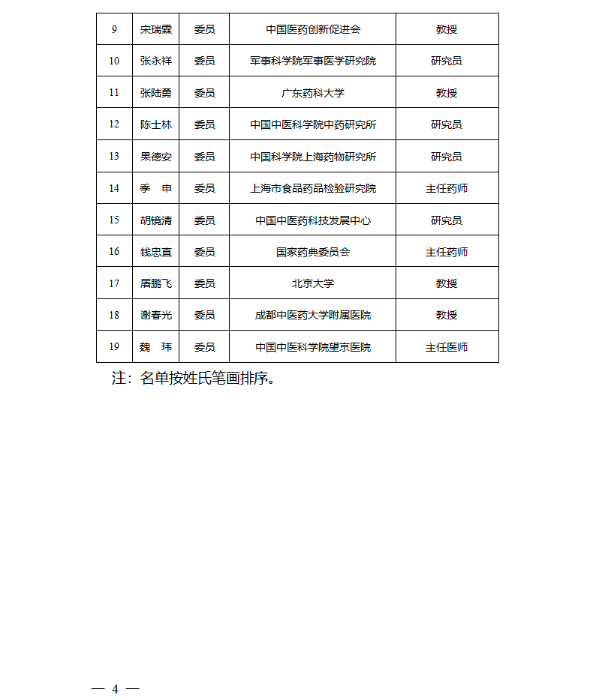
小编注意到,专委会共有40名专家,其中中科院院士2人,中国工程院院士16人,国医大师3人,资深专家19人。
其中,有企业背景的有来自云南白药集团的朱兆云院士、康缘药业的肖伟院士、河北省中西医结合医药研究院的吴以岭院士。
国家药监局此举,是为了进一步构建完善符合中药特点的审评审批体系,保障和促进中药监管工作重大决策的科学性、权威性。
小编注意到,自2020年7月1日起施行的《药品注册管理办法》中规定:
第十七条 药品审评中心等专业技术机构根据工作需要建立专家咨询制度,成立专家咨询委员会,在审评、核查、检验、通用名称核准等过程中就重大问题听取专家意见,充分发挥专家的技术支撑作用。
此前,国家药监局于2021年在对十三届全国人大四次会议第2229号建议的答复时总结了近年来建立审评专家咨询委员会的历程:
2016年成立了一致性评价专家委员会;
2017年印发《关于发布药品注册审评专家咨询委员会管理办法(试行)的公告》,规范了专家委员会工作程序,建立了12个通用专家咨询委员会、10个中药治疗领域专家咨询委员会、16个化药和生物制品治疗领域专家咨询委员会;
2017年发布了《医疗器械技术审评专家咨询委员会管理办法》,正式建立了医疗器械技术审评专家咨询制度,设立医疗器械技术审评咨询委员会。
种种作为背后,是国家药监局的重要战略部署。国家药监局曾发布通告称,2021年1到11月,国家药监局在紧急批准清肺排毒颗粒、化湿败毒颗粒、宣肺败毒颗粒的基础上,又批准了6个中药新药上市,成为近5年来获批中药新药最多的一年,中药审评审批制度改革已初显成效。
2022年6月1日,国家药监局发布《2021年度药品审评报告》。
报告提及,2021年受理审评审批的注册申请7051件,以药品类型统计,中药注册申请430件,同比增长40.07%;化学药注册申请4800件,同比增长17.50%,占全部审评审批的注册申请受理量的68.08%;生物制品注册申请1821件,同比增长39.75%。
2019-2021年,中药新药临床试验申请(IND)申请量(17件、24件、52件)、批准量(15件、28件、34件)和生物类似药上市许可申请(NDA)申请量(3件、6件、14件)、建议批准量(2件、4件、14件)均呈现连年增长的态势。2019-2021年中药IND申请量、批准量和NDA申请量、建议批准量详见下图。
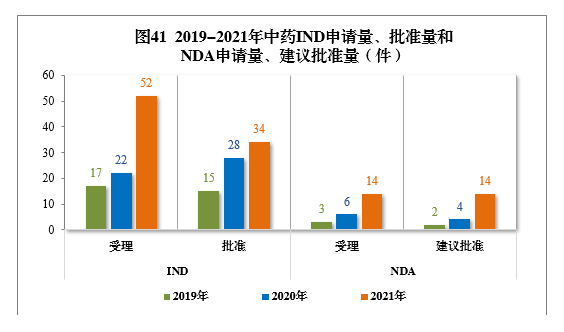
由此,报告提出,要加快推动中药审评审批机制改革:完善中药审评审批机制,加快构建以中医药理论、人用经验和临床试验相结合的中药审评体系;推进中药技术指导原则制修订,建立完善符合中药特点的审评体系,促进中药传承创新发展;加快组建古代经典名方中药复方制剂专家审评委员会。
2021年11月,国家药监局在关于政协第十三届全国委员会第四次会议第3945号(医疗体育类411号)提案答复的函中提及,要积极推动中药审评审批改革,不断总结改革成果经验和实践规律,积极构建中医药理论、人用经验和临床试验相结合的审评证据体系。
其中,对具有人用经验的中药复方制剂,适当减免药效学试验。若人用经验对有效性具有一定支撑作用,处方组成、工艺路线、临床定位、用法用量等与既往临床应用基本一致的,则可不提供药效学试验资料。中药复方制剂,根据其处方来源及组成、人用安全性经验、安全性风险程度的不同,提供相应的毒理学试验资料,若减免部分试验项目,应提供充分的理由。
来源 | 国家药监局、健康界
版权归原作者所有,若有违规、侵权请联系我们
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。
